- 제목
- 최강열.김영수 교수팀, 혁신형 알츠하이머 치료제 개발 전략 제시
- 작성일
- 2023.07.11
- 작성자
- 생명시스템대학
- 게시글 내용
-
최강열‧김영수 교수팀, 혁신형 알츠하이머 치료제 개발 전략 제시
윈트신호전달계 활성 억제를 새로운 발병 원인으로 규명
CXXC5 제어를 통한 새로운 패러다임의 신약 개발 가능성 시사

[사진. (왼쪽부터) 생명공학과 최강열 교수, 약학과 김영수 교수, 생명공학과 윤민근 박사]
생명시스템대학 생명공학과 최강열 교수, 약학대학 약학과 김영수 교수 연구팀은 윈트신호전달계(Wnt signaling pathway)의 음성되먹임인자인 ‘CXXC5’가 알츠하이머 발병을 유발하는 근본 원인 인자임을 발견하고, 윈트신호전달계를 회복시켜 작동하는 경구용 알츠하이머 혁신형 신규 물질을 개발했다. 연구 결과는 6월 22일 ‘약리학연구(Pharmacological Research, IF 10.334)’에 온라인 게재됐다(제1저자 생명공학과 윤민근 박사).
새로운 패러다임의 알츠하이머 신약 개발 필요성
알츠하이머병은 퇴행성 뇌질환의 일종으로, 인구 고령화에 따라 사회적 문제로 대두되고 있다. 현재 알츠하이머병의 원인은 신경세포 겉에 아밀로이드베타(amyloid-β)의 축적, 신경세포 내에 타우(Tau) 단백질 과인산화로 인한 신경세포 소실과 엉김, 염증 반응, 또한 최근에는 제2형 당뇨병으로 인한 뇌의 인슐린 저항성 증가 등 대사이상이 주요 원인으로 보고되고 있다.
하지만 아직 알츠하이머의 구체적이고 명확한 직접 원인은 밝혀지지 않았다. 아밀로이드베타를 타깃으로 한 항체 치료제 등 알츠하이머의 주요 원인으로 밝혀진 인자들을 타깃으로 하는 물질들은 효능과 안전성 문제로 인해 대부분 개발에 실패했고, 조건부로 승인된 치료제가 있으나 현재로서는 근본적인 치료 효과를 보이는 치료제가 없는 상황이다.
따라서 알츠하이머 치료제에 대한 의학적 미충족 수요가 매우 높고 이에 대한 새로운 패러다임의 신약 개발, 특히 새로운 메커니즘을 타깃으로 하는 치료제 개발이 절실한 상황이다. 국내외 글로벌 제약회사에서 치료제 개발 시도가 활발히 이뤄지며 그 시장성 또한 크게 증가하고 있다.
윈트신호전달계는 발생 및 손상된 조직 재생에 관련되는 중요한 신호전달계로, 알츠하이머 환자의 조직 세포에서 억제돼 있어 이 신호전달계를 타깃으로 하는 치료제 개발은 매력적으로 여겨져 왔다. 그러나 안전하게 윈트신호를 회복시키는 방법이 제시되지 못해 한계로 남아 있었다.
윈트신호전달계의 활성 억제가 알츠하이머의 원인
이번 연구에서 연구진은 ‘CXXC5’라는 윈트신호전달계의 음성되먹임 조절인자(negative feedback regulator)가 알츠하이머 환자의 뇌 조직에서 증가되는 것이 중요한 질환 원인임을 발견했고, 그 기능을 제어해 안전하게 윈트신호를 활성화시키는 혁신 알츠하이머 치료제 개발 방법을 제시했다.
구체적으로 연구진은 알츠하이머 환자와 5xFAD 알츠하이머 모델 생쥐의 해마(hippocampus) 및 전액골 피질(prefrontal cortex) 등에서 CXXC5가 크게 증가돼 있음을 발견했다. 특히 알츠하이머 환자와 5xFAD 모델 생쥐의 뇌 조직에서 윈트신호 활성을 대변하는 β카테닌(β-catenin)과는 반대로, CXXC5의 양이 Th S, GABA, Iba-1과 같은 질환 마커와 비례적으로 증가한다는 결과는 CXXC5와 알츠하이머 질환의 관계를 구체화해 준다.
연구진은 이어진 메커니즘 연구를 통해 CXXC5에 의한 윈트신호전달계의 억제를 알츠하이머병의 근본 원인으로 밝혔다. 또한, 5xFAD 알츠하이머 모델 생쥐의 노화가 진행됨에 따라 뇌 조직에서 CXXC5가 서서히 증가하면서 윈트신호 활성이 감소되는 것을 관찰함으로써, CXXC5의 과발현에 의한 윈트신호전달계의 활성 억제가 알츠하이머병의 원인임을 더욱 확실히 했다.
연구진은 CXXC5가 소실된 생쥐와 5xFAD 생쥐를 교배해 Cxxc5-/-/5xFAD 생쥐를 제조해 분석했다. 그 결과 이 생쥐는 아밀로이드베타 등 플라크 축적, 신경 염증 등 알츠하이머 마커가 개선 혹은 사라지는 것을 확인했다(그림 1).
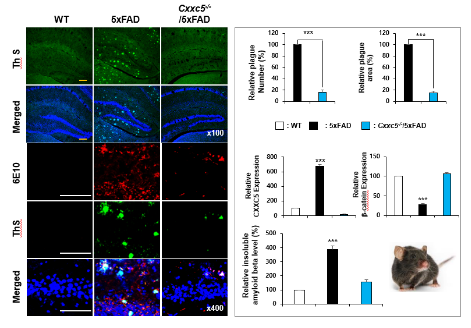
[그림 1. 5xFAD 알츠하이머 모델 생쥐와 CXXC5 유전자를 제거한 생쥐를 교배한 Cxxc5-/-/5xFAD 생쥐는 알츠하이머 표현형이 사라진다. WT, 5xFAD, Cxxc5-/-/5xFAD 생쥐의 해마 조직에서 Th S, 6E10을 면역 조직 방법을 통해 감지한 결과]
이와 더불어 Cxxc5-/-/5xFAD 교배 생쥐의 경우, 각종 마커를 통해 살펴본 결과 알츠하이머 인자들이 크게 회복된 것을 확인했다. 이 같은 결과를 통해 CXXC5의 기능을 제어함으로써 근본적인 알츠하이머 치료가 가능할 것을 예측할 수 있다.
저분자화합물 ‘KY19334’를 활용한 윈트신호 활성 전략
연구진은 이를 토대로 CXXC5가 디셰빌드(Dishevelled; Dvl)라는 윈트신호전달계 상위 단계에서 작용하는 단백질에 결합해 윈트신호전달계의 활성을 저해하는 점에 착안해, 연구진이 오랫동안 개발해 온 CXXC5-Dvl 단백질-단백질 결합(protein-protein interaction; PPI)을 저해하는 ‘KY19334’와 같은 화합물을 이용하면 알츠하이머병 환자에서 억제된 윈트신호전달계를 회복시켜 ADAM10, NeuroG1, NeuroD1, GLP-1, WISP1과 같은 타깃 유전자 발현을 정상으로 회복시켜 알츠하이머를 회복시키는 전략을 제시했다(그림 2).
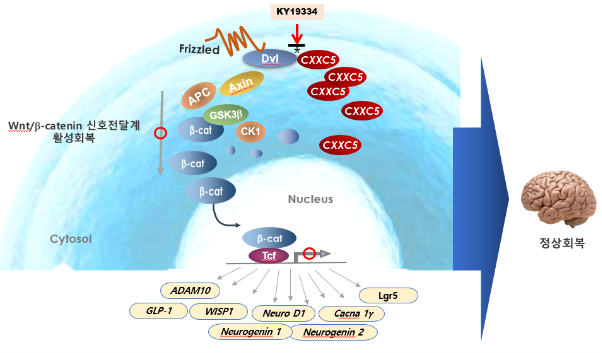
[그림 2. CXXC5-Dvl 단백질-단백질 결합 제어를 통한 알츠하이머 치료제 개발 전략. CXXC5-Dvl 단백질-단백질 결합을 저해하는 저분자화합물 ‘KY19334’를 이용해 CXXC5의 기능을 저해하면, 알츠하이머에서 억제된 윈트신호 활성이 회복되고 각종 뇌 신경과 조직 재생 유전자들의 발현 회복을 통한 치료 효과를 기대할 수 있다.]
KY19334를 알츠하이머 표현형이 나타나는 시기의 5xFAD에 4주간 경구 투여한 결과, 아밀로이드베타의 축적이 크게 줄었고, Th S와 6E10 등 마커들이 회복됐다.
또한 Y-maze, Morris water maze(MWM), Contextual fear conditioning(CFC) 등의 행동 지표들이 모두 정상 수준으로 회복된 것을 확인했다(그림 3). 이로써 저분자화합물 KY19334가 다양한 알츠하이머 표현형 질환을 개선하는 경구용 알츠하이머 치료제로서 개발될 수 있는 가능성을 입증했다.
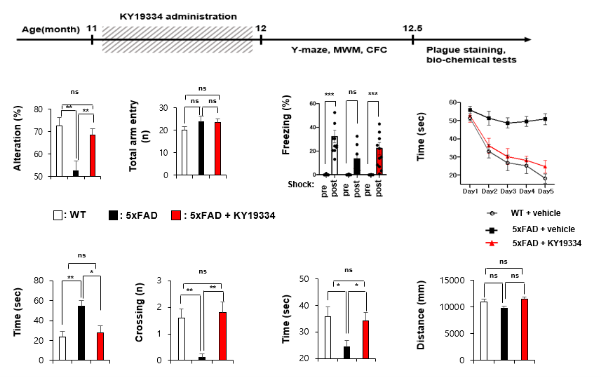
[그림 3. 정상(WT)과 알츠하이머 표현형이 나타나는 5xFAD 생쥐에 vehicle 혹은 KY19334를 25mpk 농도로 경구 투여해 각종 행동 실험을 실시한 결과. KY19334를 경구 투여한 5xFAD 알츠하이머 모델 생쥐의 알츠하이머 행동 이상이 정상에 가까이 돌아온 것을 확인했다.]
이와 같은 알츠하이머 표현형의 개선은 CXXC5-Dvl 단백질-단백질 결합 억제를 통해 회복된 윈트신호 활성을 통해 조직 재생 및 신경 발생 인자들의 유전자 발현을 회복시킨 것에 기인하며, 향후 CXXC5의 기능을 제어하는 새로운 패러다임의 알츠하이머 치료제 개발 가능성을 시사한다.
논문정보
● 논문제목: Inhibition of CXXC5 function rescues Alzheimer’s disease phenotypes by restoring Wnt/β-catenin signaling pathway